LAPORAN PRAKTIKUM FITOKIMIA
“ISOLASI DAUN PEGAGAN”
NAMA :
AUDREY DHINDA LARA
NIM :
F1F117013
GOL/KEL :
II/II
PROGRAM STUDI FARMASI
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS JAMBI
2020
PERCOBAAN V
ISOLASI
DAUN PEGAGAN (Centella asiatica)
I.
Tujuan
Mahasiswa
memahami dan melakukan isolasi senyawa golongan triterpenoid dari daun pegagan
(Centella asiatica).
II.
Landasan Teori
Senyawa metabolit sekunder biasanya terdapat
dalam organisme dalam jumlah yang sangat sedikit. Oleh karena itu biasanya
dalma proses isolasi dimulai dari sampel yang jumlahnya banyak, minimal 2 kg
samoel kering yang sudah dihaluskan. Pekerjaan isolasi membutuhkan keterampilan
dan pengalaman dalam memadukan berbagai teknik pemisahan. Untuk mendapatkan
senyawa murni biasnya peneneliti menggunakan beberapa teknik ekstraksi dan
kromatoografi. Teknik ekstraksi senyawa organic bahan alam yang biasa digunakan
antara lain maserasi, perkolasi, infudasi dan sokletasi. Sedangkan teknik
kromatografi yang biasanya digunakan antara lain adalah kromatografi lapis
tipis (KLT), kromatografi kolom vakum (KCV), kromatografi kolom gravitasi
(KKG), dan kromatotron (Centrifugal
Chromatography). Pemilihan jenis metoda biasanya dilakukan berdasarkan
pengalamn peneliti maupun hasil penelitian yang telah dilaporkan sebelumnya.
Langkah pertama yang biasnya dilakukan dalam isolasi senyawa organic bahan alam
adalah ekstraksi sampel menggunakan pelarut organic, adapun macam-macam pelarut
yang biasa digunakan adalah methanol dan etanol pada proses ekstraksi
menggunakan cara maserasi, sedangkan infusdasi biasanya menggunakan pelarut
air. Kemudian dekoksi yaitu sama dengan infusdasi hanya saja membutuhkan waktu
yang lebih lama. Langkah berikutnya setelahh diperoleh ekstrak dalam isolasi
senyawa organic bahan alam adalah ppemisahan komponen-komponen yang terdapar
dalam ekstrak tersebut. teknik yang banyak digunakan adalah kromatografi.
Kromatografi adalam teknik pemisahan campuran berdarakan perbedaan kecepatan
perambatan komponen dalam medium tertentu (Atun, 2014).
Ekstraksi adalah proses penarikan komponen
aktif (minyak asiri) yang terkandung dalam tanaman menggunakan bahan pelarut
yang sesuai dengan kelarutan komponen aktifnya. Untuk minyak asiri, proses
ekstraksi hhanya dilakukan untuk bunga-bungaan sepe rti
bunga mawar, sedap malam, lavender, geranium atau melati yang umumnya
mengandung minyak dalam jumlah yang relative kecil, komponennya mudah rusak
dengan pemanasan, dan larut dalam air. Ekstraksi minyak asiri dapat dilakukan
dengan tiga cara, yaitu ekstraksi dengan pelarut uap, ekstraksi dengan lemak
dingin dan ekstraksi dengan lemak panas. Ekstraksi dengan pelarut menguap lebih
menguntungkan dan juga lebih murah untuk biayanya, tetapi prosesnya tidak mudah
diterapkan dibandingkan dengan cara penyulingan (Satuhu dan Yulianti, 2012).
Menurut
ITIS (2020), klasifikasi ilmiah tanaman pegagan ialah sebagai berikut :
·
Kingdom : Plantae
·
Subkingdom : Viridiplantae
·
Infrakingdom : Streptophyta
·
Superdivisi : Embryophyta
·
Divisi :
Tracheophyta
·
Subdivisi : Spermatophytina
·
Kelas :
Magnoliopsida
·
SuperOrdo : Asteranae
·
Ordo :
Apiales
·
Famili :
Apiaceae
·
Genus :
Centella L.
·
Spesies : Centella
asiatica (L.) Urb.
Maserasi
adalah proses ekstraksi yang menggunakan pelarut dingin, tanpa perlakuan suhu
dan dengan cara perendaman. Cara ini paling sering digunakan, karena memiliki
beberapa kelebihan walaupun juga memiliki beberapa kekurangan. Kelebihan
ekstraksi dengan maserasi adalah senyawa yang mudah rusak akan terjaga dengan
baik karena tidak menggunakan suhu tinggi pada saat ekstraksi. Jumlah sampel
yang digunakan dapat dilakukan dengan jumlah sampel yang banyak, karena
wadahnya dapat dimodifikasi sesuai dengan jumlah sampel. Tidak menggunakan
peralatan khusus, sedangkan kekurangnnya adalah pelarut yang digunakan lebih
banyak dikarenakan perendaman yang berulang-ulang. Waktu yang diperlukan untuk
proses ekstraksi relative lebih lama. Biasanya satu kali maserasi dilakukan dalam
masa 3 hari. Jika maserasi dilakukan berulang-ulang 3 kali, maka akan
memerlukan waktu yang lama. Jika waktu yang digunakan tidak maksimuum, maka
tidak semua senyawa terekstrak dengan sempurna (Saidi et al., 2018).
Pegagan adalah
salah satu spesies tumbuhan yang belum banyak diteliti kandungan metabolit
sekundernya serta kegunaan secara ilmiah. Secara tradisional, Pegagan digunakan
sebagai obat anti infeksi, anti racun, penurun panas, peluruh air seni
(diuretikum), anti lepra, dan anti sifilis. Daunnya digunakan untuk astrigensin
dan tonikum. Pegagan mampu merevitalisasi tubuh dan otak yang lelah. Selain
itu, mampu memperbaiki sirkulasi tubuh dengan revitalisasi pembuluh darah dan
memperbaiki kesuburan wanita. Pegagan juga digunakan sebagai obat kardio
depressant, hipotensif, dan malaria. Salah satu metabolit sekunder yang
terkandung dalam tumbuhan Pegagan adalah triterpena. Triterpenoid merupakan
senyawa yang banyak terdapat dalam tumbuhan. Triterpena termasuk dalam kelompok
senyawa terpenoid. Kata terpena mencakup sejumlah besar senyawa tumbuhan, dan
istilah ini digunakan untuk menunjukkan bahwa secara biosintesis semua senyawa
tumbuhan itu berasal dari senyawa yang sama, yaitu dari molekul isopren.
Pegagan memiliki kandungan kimia seperti saponin triterpen (asiatikosida,
brahmosida, thankunusida)
dan alkaloid (hidrokofilin), isothankusida, madekasosida, brahmasida, asam
brahmik, asam modasiatik. Selain itu, terdapat juga meso-inisitol, sentelloso,
karotenoid, garam K, Ne, Ca, Fe, velarin, fatin, musilago, resin, pectin, gula
dan vitamin B (Howan, 2017).
Pegagan (Centella asiatica) merupakan tanaman
yang sejak dulu digunakan sebagai obat kulit, meningkatkan ketahanan tubuh
(panjang umur), membersihkan darah, dan memperbaiki gangguan pencernaan. Efek
farmakologis dari pegagan diantaranya sebagai anti infeksi, anti racun, penurun
panas, peluruh air seni, anti lepra, anti sipilis, anti pikun, untuk membantu
mengatasi stress serta dapat sebagai revitalitas tubuh dan otak otak yang
lelah, untuk kesuburan wanita, serta
sebagai anti pikun. Pegagan mempunyai rasa manis dan bersifat sejuk. Kandungan
bahan kimia pegagan yaitu asiatikosida, madekosida, brahmosida, tannin, resin,
pektin, gula, vitamin B, garam mineral seperti kalium, natrium, magnesium,
kalsium, besi, fosfor, minyak atsiri, pektin dan asam amino. Konstituen utama
yang terkandung di dalam daun pegagan adalah saponin asiatikosida (Dewi et al., 2018).
Isolasi
senyawa kimia dari bahan alam adalah sebuah usaha bagimana caranya memisahkan
senyawa yang bercampur sehingga dapat menghasilkan senyawa tunggal yang murni.
Tumbuhan mengandung ribuan senyawa yang dikategorikan sebagai metabolit primer
dan metabolit sekunder. Biasanya proses isolasi senyawa dari bahan alam ini
mentargetkan untuk mengisolasi senyawa metabolit sekunder, karena senyawa
metabolit sekunder diyakini dan telah diteliti dapat memberikan manfaat bagi
kehidupan manusia. Antara lain menfaatnya dalam bidang pertanian, kesehatan dan
pangan. Metode ini umum diigunakan karena senyawa organic yang diperoleh dengan
kuantitas yang cukup banyak. Tetapi berbeda dengan senyawa bahan alam hasil
proses metabolit sekunder lainnya yang pada umumnya dengan kandungan yang
relatif kecil (Marpaung, 2020).
III. Prosedur Percobaan
3.1. Alat dan Bahan
a.
Alat
-
Timbangan
analitik
-
Botol
maserasi
-
Gelas
ukur
-
Batang
pengaduk
-
Erlenmeyer
-
Beaker
glass
-
Rotarty evaporator
-
Hot plate
-
Corong
kaca
-
Botol
vial/flacon
-
Plat
tetes
b.
Bahan
-
Simplisia
daun pegagan
-
Methanol
70%
-
Akuades
-
Kertas
saring
-
Plat
KLT
-
Asam
asetat anhidrat
-
Asam
sulfat pekat (H2SO4)
3.2. Skema Kerja
IV. Hasil dan Pembahasan
Pada percobaan kali ini telah dilakukanlah praktikum
mengenai isolasi dari tanaman pegagan atau dengan nama latin yaitu Centella asiatica. Sebenarnya percobaan
ini tidak dilakukan dikarenakan kondisi yang terbatas saat ini, akibatnya hanya
dibuat dengan membahas jurnal. Pengambilan senyawa aktif pada tanaman biasa
dilakukan untuk mendapatkan senyawa tertentu yang diinginkan yang terdapat pada
tanaman tersebut, sehingga dilakukan proses isolasi. Seperti menurut Marpaung
(2020), yang mengatakan bahwa isolasi senyawa kimia dari bahan
alam adalah sebuah usaha bagimana caranya memisahkan senyawa yang bercampur
sehingga dapat menghasilkan senyawa tunggal yang murni. Untuk melakukan proses
isolasi biasanya dilakukan dengan beberapa tahapan yaitu :
- Ekstraksi
- Pemekatan
- Fraksinasi atau pemisahan
- Identifikasi
Sebelum dilakukan proses ekstraksi biasanya dilakukanlah
preparasi sampel atau penyiapan sampel. Sampel yang digunakan pada penelitian
ini ialah berupa simplisia kering daun pegagan yang kemudian diserbukkan. Tujuan
dilakukan penyerbukan adalah untuk memperkecil ukuran partikel simplisia
sehingga luas permuukaan partikel menjadi besar sehingga cairan penyari yang
akan mudah melarutkan senyawa aktif dari simplisia tersebut.
Kemudian pada percobaan ini dilakukanlah proses ekstraksi
yaitu suatu proses pemisahan atau penarikan suatu senyawa metabolit sekunder
dari sampel tanaman baik sampel kering maupun sampel basah dengan menggunakan
pelarut tertentu. Seperti menurut Widiyanto et
al., (2013), menyatakan bahwa
ekstraksi adalah metode untuk memisahkan suatu komponen dari
campuran dengan menggunakan pelarut sebagai tenaga pemisah. Ada dua teknik
pengambilan oleoresin (bahan aktif) dalam bahan rempahrempah yaitu, ekstraksi langsung
maupun gabungan antara distilasi dan ekstraksi. Pada ekstraksi langsung bahan
diekstrak menggunakan pelarut yang mudah menguap atau biasa disebut ekstraksi
maserasi. Faktor yang mempengaruhi laju ekstraksi yaitu, persiapan bahan
sebelum ekstraksi, ukuran partikel, pelarut, metode yang digunakan dalam
ekstraksi , suhu, waktu, serta proses
pemisahan pelarut dengan hasil ekstrak. Hal tersebut yang melatarbelakangi
penelitian untuk mencari perlakuan ekstraksi maserasi yang berupa variasi
ukuran bahan, suhu ekstraksi serta lama ekstraksi.
Ekstraksi yang digunakan pada penelitian ini ialah metode
maserasi dengan menggunakan pelarut campur yaitu etanol 96% dan air dengan
perbandingan 70:30. Sebelum dilakukan maserasi, terlebih dahulu dilakukan
proses deffating yaitu penghilangan lemak dengan menggunakan pelarut n-heksan. Maserasi dilakukan selama 3
hari dengan terlindung dari cahaya matahari dan dengan proses pengadukan. Hal ini bertujuan agar pelarut tidak menguap
dan menghindari oksidasi dengan udara luar. Pengadukan bertujuan untuk
menghasilkan rendemen lebih besar hal ini disebabkan karena kontak yang lebih
sering terjadi antara sampel dan pelarut dengan adanya pengadukan yang
kontinyu. Semakin banyak pengadukan maka semakin banyak desakan antara pelarut
dengan sel pada sampel sehingga semakin banyak senyawa organic yang terlarut
dalam pelarut. setelah 3 hari dilakukan re-maserasi selama 2 hari. Kemudian
hasil maserat yang didapat dipekatkan dengan menggunakan alat bernama Rotary evaporator untuk menghilangkan
atau menguapkan pelarutnya tersebut sehingga didapatkan ekstrak kental.
Pemekatan dilakukan dengan menggunakan suhu 40°C.
Sebelum dilakukan fraksinasi pada ekstrak kental, maka
dilakukan terlebih dahulu skrining fitokimia pada ekstrak daun pegagan tersebut.
Menurut Kristanti et al., (2019),
menyatakan bahwa skrining fitokimia merupakan tahap pendahuluan dalam
penelitian fitokimia. Secara umum dapat dikatakan bahwa metodenya sebagian
besar merupakan reaksi pengujian warna dengan suatu pereaksi warna. Dikarenakan
pada jurnal ini metabolit sekunder yang ingin diisolasi dari daun pegagan ini
adalah saponin, maka pada skrining fitokimia ini hanya dilakukan pengujian
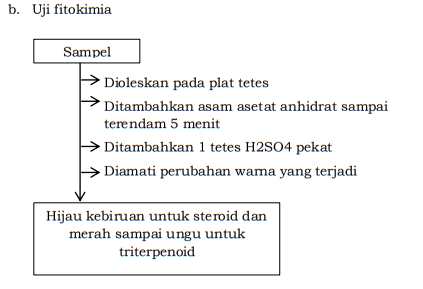
identifikasi saponin dan uji triterpenoid dan steroid. Menurut Harborne (1987),
saponin adalah senyawa dalam bentuk glikosida yang tersebar luas pada tumbuhan
tingkat tinggi. Saponin membentuk larutan koloidal dalam air dan membentuk busa
yang mantap jika dikocok dan tidak hilang dengan penambahan asam. Dan menurut
Depkes RI (1989), bahwa pengujian saponin dilakukan dengan mengocok serbuk
simplisia yang telah ditambahkan air panas selama 10 detik. Jika terbentuk busa
setinggi 1 sampai 10 cm yang stabil tidak kurang 10 menit dan tidak hilang
dengan penambahan HCl 2N menunjukan adanya saponin. Dari hasil didapatkan lah
bahwa ekstrak kental daun pegagan ini memiliki senyawa saponin ditunjukkan
dengan adanya busa. Kemudian juga dilakukan uji triterpenoid dan steroid dengan
menggunakan pereaksi Liebermann-Bouchard. Untuk mengetahui adanya senyawa terpenoid
dalam suatu sampel dapat digunakan pereaksi lieberman-burchard (anhidrida asam
asetat dan H2SO4 pekat) Hasil positif ditunjukkan apabila terbentuk cincin
berwarna merah-keunguan pada batas lapisan untuk triterpenoid dan hijau untuk
steroid. Dan didapatkan hasil bahwa pada daun pegagan ini hanya memiliki
senyawa triterpenoid.
Setelah
dilakukan identifikasi menggunakan skrining fitokimia untuk memastikan adanya
senyawa saponin pada ekstrak daun pegagan kemudian dilanjutkan dengan melakukan
fraksinasi. Fraksinasi adalah suatu proses penarikan senyawa pada sampel dengan
menggunakan 2 pelarut yang tidak bercampur. Pada jurnal ini metode fraksinasi
yang digunakan ialah menggunakan kromatografi, yaitu fraksinasi dengan teknik
pemisahan metabolit sekunder berdasarkan perbedaan migrasi komponen tersebut
dari fase diam ke fase gerak. Dan kromatografi yang digunakan ialah
kromatografi kolom dengan menggunakan fase diam berupa silica gel dan fase gerak
berupa pelarut campuran yaitu kloroform:methanol:air dengan perbandingan
30:10:1 dan didapatkan lah 39 fraksi yang selanjutnya akan di subfraksinasi
menggunakan kromatografi lapis tipis (KLT) preparative untuk pengambilan
senyawa saponin yang lebih spesifik. Fase gerak yang digunakan pada KLT ini
ialah Kloroform : methanol : air dengan perbandingan 65:25:4 dengan menggunakan
fase diam berupa silica gel GF254, dan dideteksi dibawah sinar UV
dengan panjang gelombang 366 nm yang sebelumnya telah diseprotkan dengan reagen
anisaldegid asam sulfat. Seperti menurut Alegantina et al., (2010), bahwa Pereaksi semprot anisaldehid-asam sulfat
merupakan pereaksi yang bersifat destruktif karena pereaksi ini memecah senyawa
pada plat KLT supaya dapat diamati oleh sinar tampak. Dan pada KLT ini
didapatkanlah hasil ditunjukan pada tabel 1.
Tabel
1. Nilai Rf masing-masing spot setelah
disemprot dengan Pereaksi Semprot AnisaldehidAsam Sulfat dan diamati dibawah UV
254nm.
|
Fraksi/Spot |
Rf |
Warna Spot |
|
|
4 |
0,45 |
Pemadaman Bercak |
|
|
5 |
0,45 |
Pemadaman Bercak |
|
|
8 |
0,5 |
Pemadaman Bercak |
|
|
10 |
0,5375 |
Pemadaman Bercak |
|
|
23 |
I |
0,79375 |
Pemadaman Bercak |
|
II |
0,875 |
Pemadaman Bercak |
|
Menurut Harwoko et
al., (2014), nilai Rf Asiatikosida, Madecassoside, Asiatic acid, dan
Madecassic acid sebesar 0,24; 0,16; 0,7;dan 0,8 secara berturut-turut. Fraksi
yang diduga mengandung saponin adalah fraksi 1, 4, 5, 8, dan 10 yang
menghasilkan spot berwarna biru dengan masing-masing nilai Rf 0,4875; 0,45; 0,45; 05; dan 0,5375 setelah
disemprot dengan anisaldehid-asam sulfat. Saponin akan memberikan warna coklat-ungu
setelah disemprot dengan pereaksi
anisaldehid-asam sulfat pada UV 366 nm. Hasil positif mengandung saponin
adalah terdapat spot warna ungu. Subfraksi yang memiliki bercak yang sama
digabungkan, dan yang positif mengandung saponin dipilih untuk dilakukan proses
pemisahan selanjutnya.
Kemudian dilakukanlah pemisahan senyawa murni saponin
dengan menggunakan KLT preparative menggunakan fase diam silika gel GF254 dan
fase gerak kloroform:methanol:air dengan perbandingan 65:25:4. Diperoleh 2 pita
setelah diamati dibawah sinar UV 254nm dan 366 nm dimana pita pertama berwarna
biru gelap dan pita kedua berwarna biru muda terang. Pita yang dihasilkan tidak
lurus, melainkan sangat bergelombang. Hal ini mungkin disebabkan oleh pengaruh
fase gerak, ukuran sampel, sifat analit dan adanya kontaminan. Pada
identifikasi plat KLTP di UV 366 nm bagian pinggir plat tidak menunjukkan
adanya pita yang berwarna. Hal ini kemungkinan disebabkan karena proses
pemanasan yang dilakukan tidak optimal. Kedua pita tersebut kemudian dikerok
untuk KLT Hasil Subfraksinasi. KLT hasil subfraksinasi dilakukan untuk
memastikan dari fraksi KLTP. Hasil yang diperoleh berasal dari pita pertama
dimana diperoleh spot berwarna biru dan
memiliki nilai Rf 0,46. Adanya
spot berwarna biru-ungu mencerminkan adanya kandungan saponin.
Setelah itu dilakukanlah identifikasi senyawa saponin
pada isolate yang didapatkan dengan menggunakan KLT 2 dimensi, dengan cara
melarutkan isolate hasil KLTP dengan methanol yang kemudian ditotolkan pada
plat dan dielusi dengan eluen dengan tingkat kepolaran dan arah yang berbeda.
KLT dua dimensi merupakan KLT yang menggunakan 2 eluen yang memiliki tingkat
kepolaran berbeda. Fase gerak pertama menggunakan campuran 6,9 mL kloroform,
2,7 mL methanol, dan 0,4 mL air. Fase gerak kedua menggunakan campuran 5,3 mL
kloroform, 2,8 mL asam asetat glasial, 1,1 ml metanol dan 0,7 mL air. Setelah
itu KLT 2 dimensi di amati dibawah sinar UV dan didapatkan hasil disajikan pada
tabel 2.
Tabel 2. Nilai Rf dari masing-masing spot dalam dua fase gerak
yang berbeda pada KLT Dua Dimensi.
|
Elusi |
Rf |
Warna Spot |
|
I |
0,5 |
Biru |
|
II |
0,71 |
Biru |
Dan dari hasil ini terlihat bahwa spot berwarna biru
dengan Rf elusi pertama yaitu 0,5 dimana hasil nilai Rf ini mendekati dengan Rf
dari senyawa madecassic acid yang
menurut James dan Dubery (2011), bahwa nilai Rf senyawa madecassic acid adalah sebesar 0,55. Dan pada elusi kedua juga
menghasilkan spot berwarna biru dengan nilai Rf sebesar 0,71, dan nilai Rf ini
mendekati nilai Rf senyawa Asiatic acid yang
menurut Harwoko et al., (2014), bahwa
senyawa Asiatic acid memiliki nilai
Rf sebesar 0,70, maka dari hasil ini dapat dikatakan bahwa ekstrak daun pegagan
ini mengandung senyawa golongan triterpenoid saponin yaitu madecassic acid dan Asiatic
acid.
Madecassic acid memiliki rumus molekul yaitu C30H48O6
dengan berat molekuk sebesar 504, 7 gr/mol yang dapat berfungsi untuk
mempercepat menyembuhan kulit dan memperbaiki jaringan kulit yang luka.
Kemudian Asiatic acid memiliki rumus
molekul C30H48O5 dengan berat molekul sebesar
488,7 gr/mold dan berfungsi untuk memperkuat barrier kulit dan dikenal kaya
akan antioksidan.
Menurut BPOM RI (2010), Pegagan (Centella asiatica (L.) Urban) mempunyai banyak manfaat. Pegagan (Centella asiatica (L.) Urban) secara
tradisional banyak digunakan untuk mengobati penyakit kulit. Pegagan (Centella asiatica (L.) Urban) juga dapat
digunakan untuk mengobati sakit perut, batuk, batuk berdarah dan disentri,
penyembuhan luka, radang, pegal linu, asma, wasir, tuberculosis, lepra, demam,
dan penambah selera makan. Dan menurut George dan Joseph (2009), mengatakan
bahwa Berdasarkan penelitian pegagan berkhasiat menyembuhkan antitumor,
peningkat memori, neuroprotektif, kardioprotektif, hepatoprotektif,
antimikroba, antioksidan, antiinflamasi, anti alergi, antipruitis.
V.
Kesimpulan
Berdasarkan percobaan tentang isolasi daun pegagan ini
dapat disimpulkan bahwa dalam proses isolasi terdapat berbagai tahapan untuk
mendapatkan senyawa metabolit sekunder diantaranya ialah proses pemilihan
sampel atau preparasi sampel, kemudian tahapan ekstraksi yaitu proses pemisahan
atau pengeluaran metabolit sekunder dari sampel dengan menggunakan pelarut
tertentu, kemudian dilanjutkan dengan proses fraksinasi yaitu proses penarikan
senyawa dari sampel dengan menggunakan 2 pelarut yang tidak saling campur, dan
dilanjutkan dengan proses pemurnian. Pada ekstrak daun pegagan ini senyawa yang
bisa diambil atau dimurnikan ialah senyawa golongan triterpenoid saponin yaitu madecassic acid dan Asiatic acid.
DAFTAR PUSTAKA
Atun, S.
2014. Metode Isolasi dan Identifikasi Struktur Senyawa Organik Bahan Alam. Jurnal Konservasi Cagar Budaya Borobudur.
8(2):53-61.
Badan POM
RI. 2010. Serial Data Terkini Tumbuhan
Obat. Pegagan (Centella asiatica L). Direktorat Obat Asli Indonesia. BPOM,
Jakarta.
Dewi, N.
L. A., L. P. S. Adnyani., R. B. R. Pratama., N. N. D. Yanti., J. I. Manibuy.,
N. K. Warditiani. 2018. Pemisahan, Isolasi, dan Identifikasi Senyawa Saponin
dari Herba Pegagan (Centella asiatica
L. Urban). Jurnal Farmasi Udayana.
7(2):68-76.
Depkes RI. 1989. Materia Medika
Indonesia jilid V. Departemen Kesehatan Republik Indonesia, Jakarta.
George, M dan L. Joseph. 2009. Anti-allergic, anti-pruritic, and
anti-inflammatory activities of Centella
asiatica extracts. African Journal of
Traditional, Complementary and Alternative Medicines. 6(4):554–559.
Harborne, J. B. 1987. Metode
Fitokimia Ed III. ITB-Press, Bandung.
Harwoko,
S., Pramono., A. E. Nugroho. 2014.
Triterpenoid-rich Fraction of Centella asiatica Leaves and in vitro Antihypertensive
Activity. International Food Research
Journal. 21(1):149-154.
Howan, D.
H. O. 2017. Isolasi dan identifikasi metabolit sekunder dari ekstrak butanol
pegagan (Centella asiatica (L)
urban). Fullerene Journ. Of Chem.
2(2): 92-95.
Integrated
Taxonomic Information System. 2020. ITIS
Report : Centella
asiatica (L.)
Urb. Diakses 25 April 2020 dari ITIS Report Taxonomic
Serial No.:29612:https://www.itis.gov/servlet/SingleRpt/SingleRpt?search_topic=TSN&search_value=29612#null.
James, J., dan I. Dubery. 2011. Identification and Quantification of
Triterpenoid Centelloids in Centella
asiatica (L.) Urban by Densitometric TLC. Journal of Planar Chromatography. 24(1):82-87.
Kristanti, A. N., N. S. Aminah., M. Tanjung., B. Kurniadi. 2019. Fitokimia. Airlangga University Press,
Surabaya.
Marpaung, R. G. 2020. Isolasi
Senyawa Kampferol dan Rhamnetin yang Terkandung pada Daun Tumbuhan Senna
(Cassia Angustifolia). Jakad Media Publishing, Surabaya.
Saidi, N., B. Ginting., Murnia., Mustanir. 2018. Analisis Metabolis Sekunder : Buku untuk Mahasiswa. Syiah Kuala
University Press, Aceh.
Satuhu, S dan S. Yulianti. 2012. Panduan
lengkap minyak asiri. Penebar Swadaya Grup, Jakarta.
Widiyanto, I., B. K. Anandito., L. U. Khasanah. 2013. Ekstraksi Oleoresin
Kayu Manis: Optimasi Rendemen dan Pengujian Karakteristik Mutu. Jurnal Teknologi Hasil Pertanian.
IV(1):7-15.


Komentar
Posting Komentar